|
TheòngsốtxuấthuyếtchínhthứcđượccấpphéplưuhànhtạiViệnhận định shanghai porto Cục Quản lý dược, trong đợt cấp phép, gia hạn giấy đăng ký lưu hành vaccine và sinh phẩm y tế này, có 1 sinh phẩm được cấp giấy đăng ký lưu hành hiệu lực 5 năm; 8 vaccine, sinh phẩm được cấp giấy đăng ký lưu hành hiệu lực 3 năm; 22 vaccine, sinh phẩm được gia hạn giấy đăng ký lưu hành hiệu lực; 9 sinh phẩm được gia hạn giấy đăng ký lưu hành hiệu lực 3 năm. 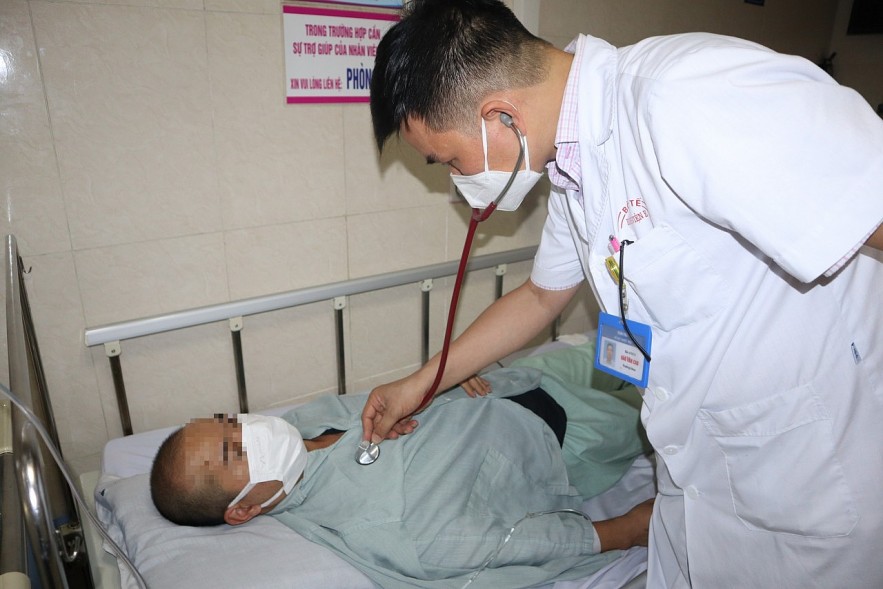 | Bác sỹ điều trị cho bệnh nhân sốt xuất huyết tại Bệnh viện E. Ảnh: TL. |
Vaccine phòng sốt xuất huyết của Takeda là một trong số 40 vavcine, sinh phẩm được cấp phép, gia hạn lần này. Vaccine sốt xuất huyết sử dụng cho người từ 4 tuổi trở lên, bất kể đã hoặc chưa từng mắc bệnh. Đây là vaccine sốt xuất huyết đầu tiên được cấp phép tại Việt Nam cho cá nhân mà không cần xét nghiệm trước khi tiêm. Bà Katharina Geppert - Tổng giám đốc Takeda Việt Nam cho rằng, Bộ Y tế Việt Nam phê duyệt vaccine phòng sốt xuất huyết là bước tiến trong nỗ lực chung phòng ngừa sốt xuất huyết, đánh dấu một cột mốc to lớn đối với Takeda và việc phòng ngừa rủi ro sức khỏe do bệnh sốt xuất huyết gây ra. "Vaccine này sẽ trở thành công cụ phòng ngừa bổ sung quản lý bệnh sốt xuất huyết toàn diện, góp phần giảm thiểu tác động của căn bệnh này. Chúng tôi sẽ tiếp tục hợp tác với các cơ quan quản lý, chuyên gia y tế, các hội chuyên môn, các viện nghiên cứu, các cơ quan Nhà nước, các tổ chức tư nhân cũng như nhiều bên liên quan khác để cùng chung tay phòng chống bệnh sốt xuất huyết tại Việt Nam và các quốc gia khác" - bà Katharina Geppert cho hay. | Tại Việt Nam, tính đến ngày 25/4, số mắc trong 4 tháng đầu năm đã là hơn 16.800 ca, 1 trường hợp tử vong. Cục Y tế dự phòng (Bộ Y tế) cho biết, xét nghiệm trên người bệnh cho thấy có cả 4 type huyết thanh gây sốt xuất huyết dengue, trong đó DEN-2 chiếm 88% tổng số ca nhiễm năm 2023 và 70% tổng số ca nhiễm năm 2024. |
|